En Paraguay, la investigación sobre la contaminación por arsénico (As) es aún incipiente. El objetivo del presente estudio fue validar un método analítico para la determinación de arsénico total en muestras de suelo por espectrofotometría de absorción atómica con generación de hidruros (EAA-GH). Para la validación se colectó una muestra blanco de un área de nula actividad antropogénica y, para su aplicación, diez muestras de la cuenca del río Tebicuary. El sistema de muestreo fue combinado por cuadrícula. Las muestras fueron secadas, tamizadas, homogeneizadas y digeridas mediante digestión asistida por microondas. La determinación se realizó por EAA-GH. Se evaluaron parámetros de desempeño analítico como selectividad, linealidad, sensibilidad, exactitud, LOD, LOQ, robustez, incertidumbre y aplicabilidad. El método aplicado fue selectivo para As total y cumplió con los criterios de aceptación; linealidad 0,2 a 12 µg·L-1 (r > 0,99), sensibilidad (m = 0,0395 ± 0,005), exactitud y precisión (%R > 95 %), repetibilidad (CV = 4,26 %), reproducibilidad (CV = 4,52 %), LOD (0,11 mg·kg-1) y LOQ (0,21 mg·kg-1). El método fue robusto ante variaciones de pH y tamaño de las partículas. De diez muestras analizadas, una tuvo concentración de As total superior a 20 mg·kg-1.
Palabras clave: digestión ácida, EAA-GH, Paraguay, contaminación.
No Paraguai, as pesquisas sobre a contaminação arsênico (As) ainda são incipientes. O objetivo deste estudo foi validar um método analítico para a determinação de arsênio total em amostras de solo por espectrofotometria de absorção atômica com geração de hidretos (HG-AAS). Uma amostra-branco foi tomada de uma área de atividade antrópica nula para a validação do método e, outras dez amostras da bacia do rio Tebicuary, para sua aplicação. A amostragem foi combinada por grade. As amostras foram secas, peneiradas, homogeneizadas e digeridas em forno de micro-ondas. A quantificação foi realizada por HG-AAS. Além disso, os parâmetros de desempenho analítico como seletividade, linearidade, sensibilidade, precisão, LOD, LOQ, robustez, incerteza e aplicabilidade, foram avaliados. O método foi seletivo para As e atendeu aos critérios de aceitação. Linearidade de 0,2 a 12 µg·L-1 (r > 0,99), sensibilidade (m = 0,0395 ± 0,005), exatidão (R > 95 %), repetibilidade (CV = 4,26 %), reprodutibilidade (CV = 4,52 %), LOD (0,11 mg·kg-1) e LOQ (0,21 mg·kg-1). O método foi robusto a variações de pH e tamanho de partícula. Das dez amostras analisadas, uma apresentou concentração do total As superior a 20 mg·kg-1.
Palavras-chave: digestão ácida, HG-AAS, Paraguai, contaminação.
Introducción
El arsénico (As) es un elemento de gran distribución en la corteza terrestre; se encuentra naturalmente en el suelo y otros compartimentos ambientales como producto de la erosión de las rocas, la precipitación y la actividad volcánica (Reid et al., 2020; El Himri et al., 2022).
A nivel mundial, al menos 120 países se ven afectados por la presencia de As en las aguas subterráneas, mientras que en América Latina el problema afecta a países como Argentina, Bolivia, Brasil, Chile, Colombia, Cuba, Ecuador, El Salvador, Guatemala, Honduras, México, Nicaragua, Perú y Uruguay (Litter et al., 2019). La distribución espacial de arsénico en América del Sur presenta ciertos vacíos que se verifican en la región que abarca Paraguay.
En el suelo, el arsénico se encuentra generalmente entre 5 y 10 mg·kg-1 como componente principal de más de 200 minerales (As nativo, arseniuros, sulfuros, óxidos, arseniatos y arsenitos). Las mayores concentraciones se hallan en sulfuros como pirita, calcopirita, galena y marcasita (Litter et al., 2009). Las altas concentraciones en los suelos representan un riesgo importante para la calidad del agua, superficial o subterránea, el desarrollo animal y vegetal, la seguridad alimentaria y, por ende, la calidad de la salud humana (Gerdelidani et al., 2021). Según la Organización de las Naciones Unidas para la Alimentación y la Agricultura (FAO) y la Agencia para Sustancias Tóxicas y el Registro de Enfermedades (ATSDR), el nivel máximo permitido de arsénico total en suelo es de 20 mg·kg-1 (Heikens, 2006; ATSDR, 2009).
En Paraguay, se han encontrado concentraciones elevadas de As en cauces hídricos de los departamentos de Canindeyú y Caazapá (Fariña et al., 2019); además se observaron niveles variables de As total en muestras de arroz (Oryza sativa) provenientes de cuencas productoras en la zona de Caapucú, Arazapé y Villa Oliva (Mereles et al., 2017).
Un método analítico confiable que permita la cuantificación del arsénico en muestras de suelo requiere ser validado para la confirmación de las aptitudes consistentes con las aplicaciones requeridas (Eurolab España, 2016). Además, es fundamental contar con un método que sea rápido, eficiente, reproducible y con reducción del uso de reactivos y muestras. La evaluación de parámetros de desempeño como linealidad, reproducibilidad, repetibilidad, límites de detección y cuantificación es importante para demostrar la correcta aplicación del método y los intervalos de variación posibles, que no afecten su desempeño ni la confiabilidad de los resultados (Duffau et al., 2010). El objetivo del presente trabajo fue validar el método analítico para la determinación de arsénico total en muestras de suelo por espectrofotometría de absorción atómica con generación de hidruros.
Materiales y Métodos
Muestreo y preparación de muestras
Para el estudio se colectaron, en 2021, muestras de suelo por el método de muestreo combinado por cuadrícula. Se extrajeron 500 g de cuatro excavaciones de una profundidad de 0 – 25 cm y se mezclaron las submuestras para obtener una muestra de aproximadamente 2 kg de suelo en bolsas de polietileno selladas (Kebonye et al., 2021).
Para los ensayos de validación del método se utilizó una muestra blanco colectada en las proximidades del lago Ypoá, al norte de la cuenca del río Tebicuary; considerada un área de nula actividad antropogénica, donde no se ha encontrado contaminación de las aguas (Fretes López y Díaz Cubilla, 2014). Mientras tanto, para la aplicación del método con muestras analíticas se colectaron muestras de diez puntos seleccionados dentro de la cuenca del río Tebicuary (Figura 1).
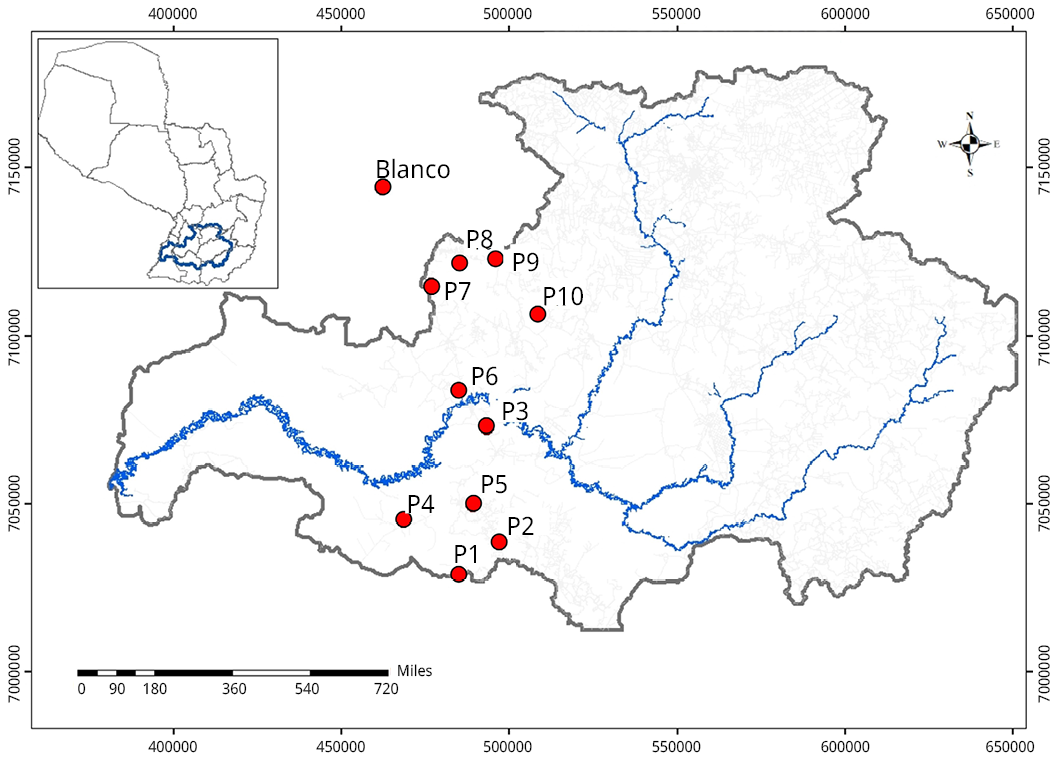
Figura 1. Puntos de muestreo de suelos colectados para la validación del método analítico.
Las muestras se secaron a temperatura ambiente (23 ± 1 ℃) hasta una variación menor al 5 % de su peso, se tamizaron a través de un tamiz de 1 mm (los terrones de suelo se disgregaron en mortero), y se almacenaron en bolsas de polietileno selladas (Zagal y Sadzawka, 2007). La reducción de la masa se realizó por cuarteo, procediéndose a pulverizar la muestra mediante el uso de un mortero de ágata, y se tamizó con tamiz de 106 µm (Litter et al., 2009).
Materiales, reactivos y equipos
La pulverización de las muestras se logró con tamices calibrados (ASTM E11, Gilson). Para pesar las muestras se utilizó una balanza analítica (Kern ALJ, 0,1 mg) y posteriormente se realizó la digestión ácida con la adición de ácido nítrico concentrado (Cicarelli, Argentina), ácido clorhídrico concentrado (Cicarelli, Argentina), ácido fluorhídrico concentrado (Biopack, Argentina) y ácido bórico (Merck, Alemania) mediante microondas (CEM, MARS2, Estados Unidos) con ciclos de digestión según lo descrito en el artículo sobre optimización del método, previamente analizado por el grupo de investigación (Diez-Pérez-Núñez et al., 2021).
Luego, las muestras digeridas fueron calentadas con plancha calefactora (Cole-Parmer, Estados Unidos) hasta reducir su volumen, con posterior agregado de ioduro de potasio (TECHNO PHARMCHEM, India) y ácido ascórbico (CICARELLI, Argentina).
La cuantificación de arsénico total se llevó a cabo por el método de espectrofotometría de absorción atómica acoplada a generación de hidruros (Shimadzu AA-6300, HVG-1, Estados Unidos), previamente calificado por el representante de la marca (Certificado Nº 1521, 05/05/2021). Los parámetros de operación del equipo fueron previamente ajustados (Diez-Pérez-Núñez et al., 2021). Se prepararon curvas de calibración de concentraciones entre 0,2 – 12 µg·L-1 a partir de la solución patrón de As (1000 mg·L-1, trazable al NIST, SUPELCO; Alemania).
Para la generación de hidruros volátiles se preparó una solución al 0,4 % con borohidruro de sodio (MP BIOMEDICALS, Estados Unidos) y 0,5 % de hidróxido de sodio (Cicarelli, Argentina). Todas las soluciones utilizadas fueron preparadas con agua ultrapura (resistividad 18 MΩ·cm-1).
Además, se utilizó el pHmetro (Oakton, Estados Unidos) y el agitador magnético (Cole-Parmer, Estados Unidos) para la medición del pH en muestras de suelo para el ensayo de robustez. La modificación del pH se realizó con la adición de carbonato de calcio sólido (Cicarelli, Argentina).
El análisis estadístico de los resultados se realizó con el software IBM SPSS Statistics (Estados Unidos) (IBM Corp., 2015). Se aplicaron estadísticos descriptivos, pruebas de Pearson, Kruskal-Wallis, U-Mann Whitney y ANOVA con un nivel de confianza de 95 %. Para la elaboración del mapa del área de estudio se utilizó el software ArcGIS 10.8.
Procesamiento de las muestras
El tratamiento de la muestra consistió en pesar 0,2000 g de suelo pulverizado (< 106 µm) en los vasos del horno digestor y posteriormente adicionar 3,5 mL de ácido nítrico (65 %), 0,5 mL de ácido clorhídrico (36,5-38 %) y 1 mL de ácido fluorhídrico (40 %). El ácido fluorhídrico fue agregado para la disolución de silicatos presentes en la muestra, que requiere aplicar un segundo ciclo de digestión para su neutralización con 0,6 g de ácido bórico, cantidad que fue establecida según ensayos preliminares de optimización del método (Vieira et al., 2005; Diez-Pérez-Núñez et al., 2021).
Una vez finalizada la digestión se redujo el volumen por calentamiento (hasta 2 mL aproximadamente) para eliminar el exceso del oxidante. El extracto concentrado se llevó a volumen de 100 mL en un matraz aforado. Posteriormente se tomó una alícuota de 5 mL y se transfirió a un matraz aforado de 50 mL, al que se le agregaron 10 mL de ácido clorhídrico 4,5 mol·L-1, 0,5 g de ácido ascórbico y 0,5 g de ioduro de potasio para obtener la reducción del As (V) a As (III), para lo cual se dejó reposar durante al menos 1 hora.
Se prepararon blancos de reactivos, consistentes en una solución cuyo contenido estaba compuesto por todos los reactivos utilizados en el procesamiento de la muestra, con los mismos volúmenes y concentraciones. Los blancos de reactivos atravesaron el proceso analítico en las mismas condiciones que las muestras y se analizaron para determinar la contribución a la señal de la medida (Eurolab España, 2016).
Validación del método analítico
El desempeño del método se evaluó mediante la prueba de selectividad, que consistió en aplicar la prueba del efecto matriz (Senila et al., 2020, Miller y Miller, 2002). Se compararon las pendientes de tres curvas de calibración elaboradas a partir de estándares puros y tres curvas de calibración de los estándares en las muestras de suelo. Las curvas fueron obtenidas graficándose las concentraciones de arsénico de 0,5; 1,0; 2,0; 4,0; 6,0 y 8,0 µg·L-1 con sus correspondientes absorbancias. Se graficó la absorbancia obtenida (eje y) en función de la concentración de As (eje x) y se calculó la ecuación de la recta. La significancia estadística se evaluó mediante la prueba U de Mann-Whitney con un nivel de confianza de 95 %.
Para evaluar la linealidad se prepararon cuatro curvas de calibración de concentraciones 0,2; 0,6; 1,0; 4,0; 8,0; 10 y 12 µg·L-1 a partir de la solución patrón de As y se calculó el coeficiente de correlación (r). El criterio de aceptación para determinar la linealidad en análisis de trazas tiene un valor igual o mayor que 0,99 (Duffau et al., 2010), así como la confirmación por inspección visual del gráfico. Además, se calculó la pendiente de las cuatro curvas, su media y la desviación estándar para estimar la sensibilidad.
La prueba de recuperación se aplicó para evaluar la veracidad ya que al momento del estudio no se disponía de material de referencia certificado de suelo, por lo tanto, se procedió con la fortificación de las muestras. Se prepararon seis muestras de suelo sin fortificar y seis muestras de suelo fortificadas en tres niveles de concentración correspondientes a nivel bajo, medio y alto (Duffau et al., 2010). Las muestras fortificadas fueron preparadas mediante el agregado del patrón de As antes del proceso de digestión, de tal manera de obtener concentraciones de 3 µg·L-1, 10 µg·L-1 y 25 µg·L-1. Con los resultados, se calculó el porcentaje de recuperación mediante la Ecuación 1.
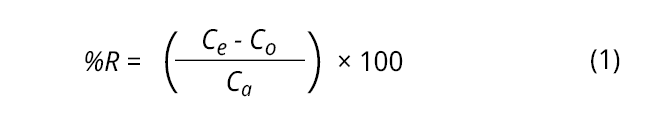
Donde Ce corresponde a la concentración del analito de la muestra enriquecida, Co a la concentración del analito medida en la muestra sin adicionar (muestra blanco) y Ca a la concentración del analito para la muestra enriquecida.
Para determinar el criterio de aceptación se calcularon los límites de control (LC) con el promedio y la desviación estándar (DS) de las recuperaciones obtenidas para distintos niveles y días (LC ± 2DS) (Miller y Miller, 2002).
Con el fin de evaluar la precisión se realizó la prueba de repetibilidad (RSd) y reproducibilidad (RSD). Para la repetibilidad se analizaron ocho réplicas independientes de muestras blanco, manteniendo en todo momento las condiciones de repetibilidad durante el proceso (mismo operador, mismo equipo, mismo laboratorio y en corto intervalo de tiempo), mientras que para el ensayo de reproducibilidad se analizaron ocho réplicas independientes con las mismas características descritas para el ensayo de repetibilidad. Sin embargo, fueron procesadas por un analista distinto y en un periodo de tiempo prolongado (Eurolab España, 2016). Posteriormente, se calculó la desviación estándar y el porcentaje de coeficiente de variación (CV %) para ambos ensayos y se evaluó mediante el coeficiente de variación de Horwitz (Duffau et al., 2010). El coeficiente de variación de Horwitz (CVh %) fue calculado para una concentración de 6,5 mg·kg-1 (concentración estimada para la muestra blanco) mediante la Ecuación 2.
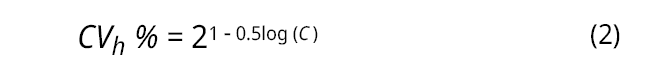
Donde C es el valor nominal del analito expresado en potencia de 10.
Como criterio de aceptación para la repetibilidad se considera que el CV % obtenido debe ser menor que CVh %/2 y para la reproducibilidad intralaboratorio debe ser menor que 2CVh %/3 (Duffau et al., 2010). Además, con las muestras blanco leídas en diferentes días se evaluó la precisión entre grupos, la precisión dentro de los grupos y la precisión intermedia del método mediante la prueba de ANOVA.
Los límites de detección (LOD) y cuantificación (LOQ) se calcularon a partir de ocho réplicas de muestras fortificadas de concentración de 0,2 µg·L-1, con los resultados obtenidos se determinó la desviación estándar (DS) utilizada para ambos cálculos. El LOD se calculó mediante el enfoque “3S”, donde LOD = 3DS, y el LOQ se calculó mediante la fórmula LOQ = 10DS (Eurolab España, 2016). Cuando el límite máximo permisible (LMP) es ≥ 0,1 ppm, el criterio de aceptación para el LOD es ≤ 1/10 LMP y para el LOQ, ≤ 1/5 LMP (Duffau et al., 2010). Cabe mencionar que el LMP considerado fue 20 mg·kg-1, establecido por la FAO (El Himri et al., 2022).
Para el ensayo de robustez se aplicó la prueba de Youden y Steiner (Duffau et al., 2010). Se prepararon ocho muestras a fin de evaluar el efecto de la variable de pH y tamaño de partícula de suelo. Como criterio de aceptación se consideró que la diferencia entre el valor alto y el valor bajo de la variable evaluada sea superior a √ 2 de la desviación estándar (Duffau et al., 2010). Los ensayos correspondientes a las muestras de 1 al 4 se procesaron en muestras control a pH 4,5 mientras que las muestras del 5 al 8, a pH 7.
El pH fue determinado en suspensión de suelo seco a temperatura ambiente (fracción < 1mm) con agua destilada en proporción muestra:agua de 1:2,5; se agitó mediante agitador magnético durante 5 minutos y se dejó reposar al menos 2 horas. Posteriormente se agitó la suspensión y se realizó la lectura del pH (Zagal y Sadzawka, 2007). En cuanto al tamaño de partícula de suelo, para los ensayos 1, 2, 5 y 6 se utilizaron muestras pulverizadas y tamizadas con tamiz de 106 µm (Litter et al., 2009) y para los ensayos 3, 4, 7 y 8 se utilizaron muestras molidas y tamizadas con tamiz de 1 mm.
En el cálculo de incertidumbre se identificaron las fuentes que influyen en el método analítico, para ello se graficó el diagrama de Ishikawa (Martínez et al., 2018, Ishikawa, 2002). Se calcularon la incertidumbre estándar, incertidumbre estándar relativa e incertidumbre combinada (Cáñez Carrasco y García Alegría, 2015). Una vez obtenida la incertidumbre combinada se multiplicó por un factor de cobertura (K = 2) a fin de entregar un 95 % de confianza, y así establecer el intervalo en torno al resultado de la medición en el cual se espera que se incluya la mayor fracción de la distribución de los valores que se pueden atribuir al mensurando (Duffau et al., 2010; Cáñez Carrasco y García Alegría, 2015).
Para la aplicabilidad se determinó la concentración de As total en diez muestras de suelo provenientes de la cuenca del río Tebicuary, las cuales fueron georreferenciadas. Los resultados obtenidos fueron expresados mg·kg-1 y se compararon con el valor de referencia (El Himri et al., 2022).
Resultados y Discusión
En base a los diferentes experimentos para la evaluación de los parámetros de desempeño, no se observó diferencia significativa para el efecto matriz (p = 0,200, U de Mann-Whitney) en la comparación de las curvas de calibración elaboradas a partir de estándares puros y curvas de calibración de los estándares en las muestras de suelo (Figura 2 a).
El método evaluado puede cuantificar el As en presencia de los interferentes que se encuentran en la matriz, confirmando que la espectrofotometría de absorción atómica con generación de hidruros es una técnica sencilla y selectiva para la determinación de As (Fernández Rodríguez, 2020).
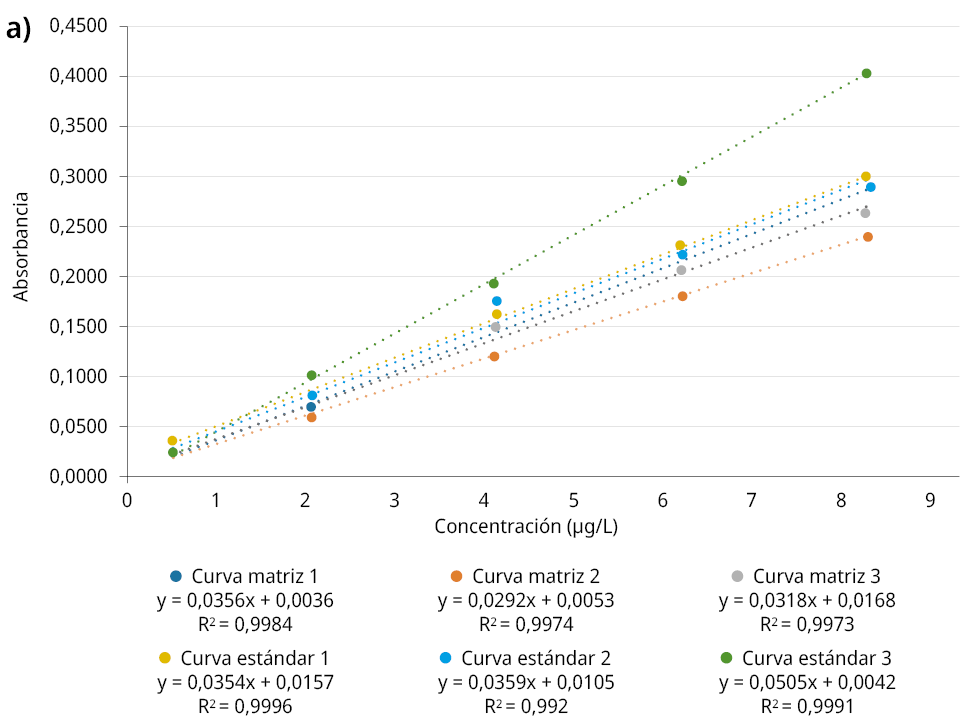
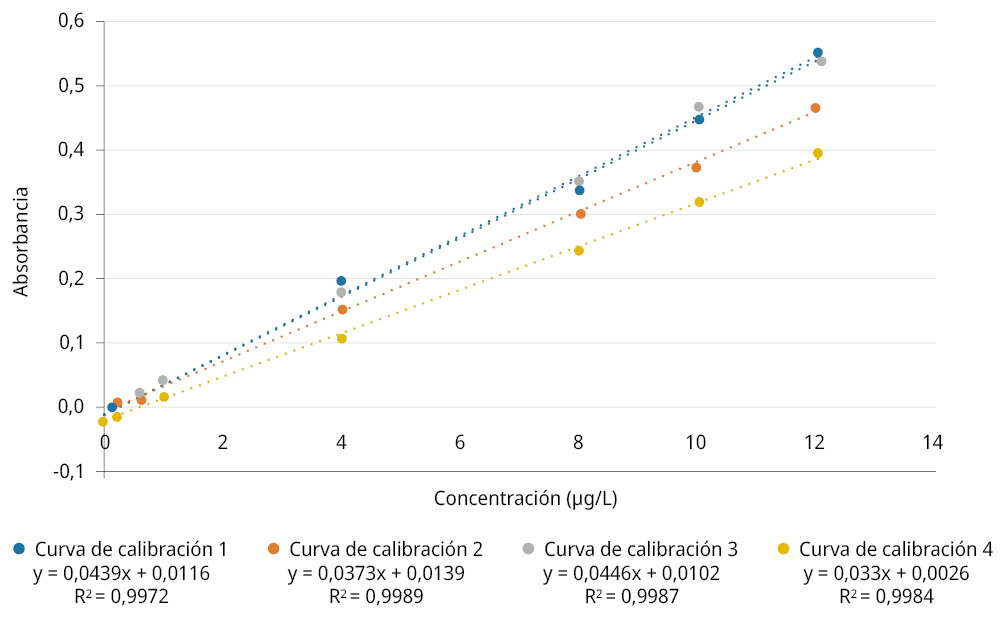
Figura 2. Evaluación del desempeño de (a) selectividad y (b) linealidad y sensibilidad.
Las curvas de calibración del estándar de As presentaron un comportamiento lineal con alto grado de correlación en el rango de concentración de 0,2 µg·L-1 a 12 µg·L-1, con coeficientes de correlación (r) entre 0,9986 - 0,9994 (Figura 2 b: el software presenta R2, por lo que se procedió a calcular r = √R2).
Los valores de r se encontraron dentro del criterio de aceptación para el análisis de trazas -igual o mayor que 0,99-, lo cual demuestra una buena linealidad para el intervalo de trabajo mencionado (Duffau et al., 2010). Además, las pendientes de las cuatro curvas de calibración realizadas presentaron valores entre 0,0330 y 0,0446, con una media de 0,0395 ± 0,005. Los resultados de sensibilidad obtenidos fueron superiores a los reportados por Rada et al. (2012) con pendientes entre 0,00361 y 0,00429 y por Tafur Yépez (2014) con una pendiente de 0,008; en ambos casos la cuantificación de As se realizó mediante espectrofotometría de absorción atómica con generación de hidruros pero en matrices distintas.
Cabe resaltar que la sensibilidad puede encontrarse afectada por el tiempo transcurrido entre la preparación de la curva de calibración y su lectura, el tiempo de estabilización previa de la señal del equipo de espectrofotometría de absorción atómica y el tiempo que transcurre desde la aspiración de la muestra hasta el registro de la señal, por lo que este proceso debería estar estandarizado de manera de tener resultados óptimos, no solo respecto a la sensibilidad sino también a la reproducibilidad del método analítico (Diez-Pérez-Núñez et al., 2021).
En el ensayo de recuperación, en tres niveles de concentración de As correspondientes a 3 µg·L-1, 10 µg·L-1 y 25 µg·L-1, el porcentaje de recuperación de las muestras de suelo fortificadas obtenidas fue de 101,44 %, 95,99 % y 108,99 %, respectivamente. Todos los resultados obtenidos se encontraron dentro del criterio de aceptación calculado 89,08 – 115,20 %. Se comprueba que, para los tres niveles de concentración analizados, el rendimiento del método analítico es satisfactorio para el fin propuesto.
El coeficiente de variación (CV, expresado como %) del ensayo de repetibilidad fue de 4,26 % y el de reproducibilidad, de 4,52 %. Ambos valores fueron aceptados debido a que cumplieron con el criterio de aceptabilidad correspondiente al coeficiente de variación de Horwitz, ya que para la repetibilidad el CV obtenido debe ser menor que CVh % / 2 (6,04 %) y para la reproducibilidad intralaboratorio debe ser menor que 2CVh % / 3 (8,06 %). La precisión entre grupos fue igual a 7,35, la precisión dentro del grupo 8,89 y la precisión intermedia del método 11,54. Como la F calc (2,36) << F crítico (3,86) no hay significancia estadística en los resultados obtenidos de las muestras analizadas (p = 0,142, ANOVA).
Los límites de detección y cuantificación fueron de 0,11 y 0,21 mg·kg-1, respectivamente. Ambos resultados fueron adecuados considerando que los criterios de aceptación para LOD y LOQ corresponden a LOD ≤ 2 mg·kg-1 y LOQ ≤ 4 mg·kg-1.
Mediante los valores obtenidos para la prueba de Youden y Steiner se evidenció la robustez del método en estudio frente a las variables analíticas pH y tamaño de las partículas. La diferencia entre los promedios del valor alto y del valor bajo fue inferior a √2 DS de las determinaciones realizadas (Tabla 1), por lo que se afirma que los resultados obtenidos no se ven afectados frente a dichas modificaciones e indican la fiabilidad del método durante su uso (Eurolab España, 2016).
Tabla 1. Resultados del ensayo para la prueba de Youden y Steiner.

Entre las fuentes de incertidumbre presentes durante el proceso analítico se encontraron la incertidumbre del material volumétrico, la masa de suelo, el factor de dilución, la solución de trabajo de As, la curva de calibración y la lectura del mensurando en el espectrofotómetro de absorción atómica con generación de hidruros (Figura 3). Los valores obtenidos de la incertidumbre expandida se encuentran incluidos en los resultados de aplicabilidad, junto con las respectivas concentraciones de As total en las muestras de suelo. El criterio de aceptación para una incertidumbre expandida aceptable corresponde a un valor < 30 % del mensurando, por lo que las incertidumbres de todas las muestras fueron aceptadas (Mencias Recalde, 2018). Además, se demuestra que la metodología propuesta permite estimar la incertidumbre del mensurando, un requisito de la ISO 17025 (International Organization for Standarization, 2017) vigente para todos los laboratorios de ensayo y calibración.

Figura 3. Diagrama de Ishikawa (2002) elaborado para el análisis de las fuentes de incertidumbre.
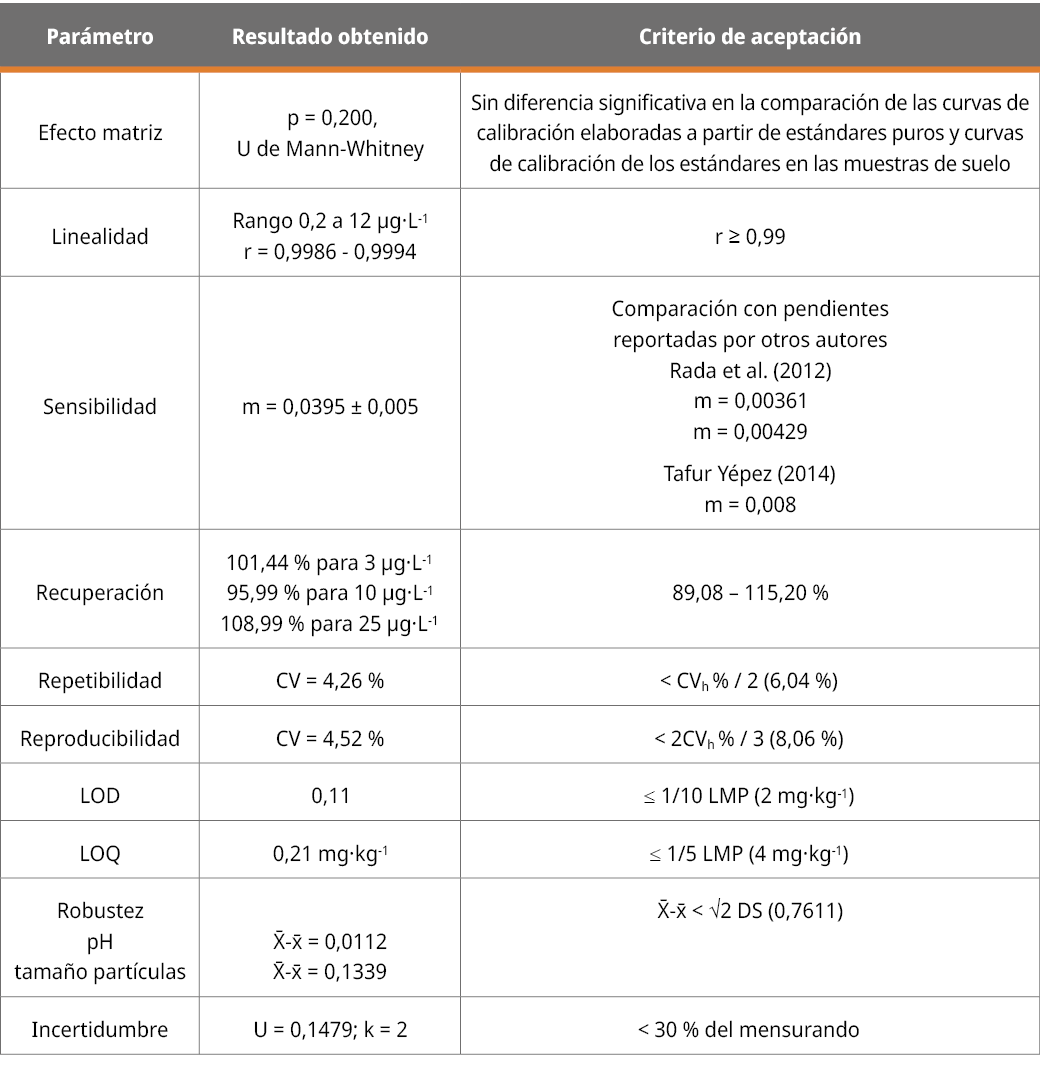
Una vez culminada la evaluación de todos los parámetros de validación, se procedió a sintetizarlos en la Tabla 2.
Tabla 2. Resumen de resultados obtenidos para la validación del método analítico.
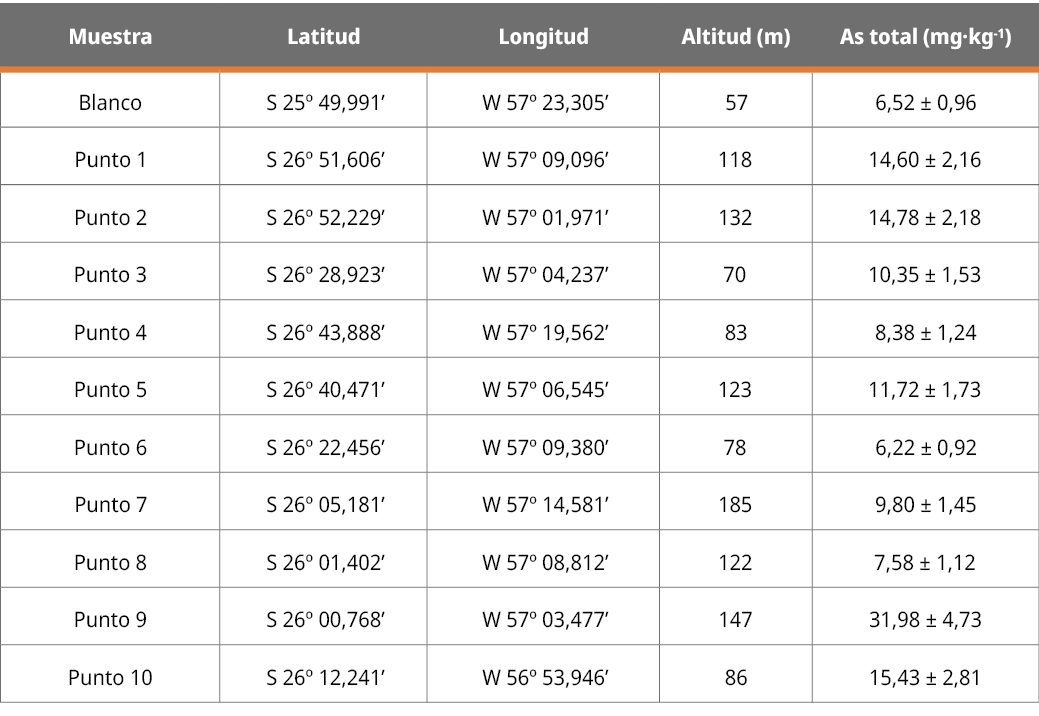
Los resultados de la concentración de As total en la muestra blanco proveniente de la zona del lago Ypoá fue de 6,5 ± 0,96 mg·kg-1, mientras que las muestras de suelo provenientes de la cuenca del río Tebicuary presentaron concentraciones entre 6,22 ± 0,92 mg·kg-1 y 31,98 ± 4,73 mg·kg-1 (Tabla 3).
Tabla 3. Concentraciones de arsénico total en muestras de suelo.
Conclusiones
Los parámetros de desempeño evaluados para la determinación de arsénico total en muestras de suelo por espectrofotometría de absorción atómica con generación de hidruros cumplieron con todos los criterios de aceptación establecidos, por lo que el método es adecuado para el fin propuesto.
Según las concentraciones de As total de las diez muestras de suelo provenientes de la cuenca del río Tebicuary, una de ellas se encontró por encima de 20 mg·kg-1, en un punto de mayor altitud (147 m sobre el nivel del mar) y aproximadamente 2 km del distrito de Ybycuí, Departamento de Paraguarí; por lo que se estima que el origen podría ser geogénico. Sin embargo, esto debe ser investigado en futuros estudios.
Agradecimientos
Este trabajo fue elaborado en el marco del proyecto PINV18-1061 “Distribución de arsénico total en la biosfera de la cuenca del río Tebicuary, Paraguay”, cofinanciado por el Consejo Nacional de Ciencia y Tecnología (CONACYT) con apoyo del FEEI.
Referencias
ATSDR, 2009. Health consultation: evaluation of environmental data [En línea]. Atlanta: ATSDR. [Consulta: 02 de junio de 2023]. Disponible en: bit.ly/441PLzt
Cáñez Carrasco, M. G. y García Alegría, A. M., 2015. Estimación de la incertidumbre en la cuantificación de fósforo por espectrofotometría ultravioleta-visible. En: Biotecnia, 17(3), pp. 34–41.
Diez-Pérez-Núñez, D.; Colmán, D.; García, L.; Nakagoe, S.; Ramírez, K.; Torres, O.; Olivares, J. C. y Mereles, L., 2021. Optimización del método de digestión por microondas y espectrofotometría de absorción atómica con generador de hidruro para la cuantificación de arsénico en diferentes matrices. En: South Florida Journal of Development, 2(5), pp. 7102–7110. DOI: https://doi.org/10.46932/sfjdv2n5-057.
Duffau, Boris; Rojas, Fabiola; Guerrero, Isabel; Roa, Luis; Rodríguez, Luis; Soto, Marcelo; Aguilera, Marisol y Sandoval, Soraya, 2010. Guía Técnica. Validación de métodos y determinación de la incertidumbre de la medición. Santiago: Instituto de Salud Pública de Chile. pp. 70.
Eurolab España, 2016. Guía Eurachem: La adecuación al uso de los métodos analíticos – Una Guía de laboratorio para la validación de métodos y temas relacionados [En línea]. Gembloux: Eurolab. [Consulta: 28 de octubre de 2020]. Disponible en: https://www.eurachem.org/images/stories/Guides/pdf/MV_guide_2nd_ed_ES.pdf
Fariña, S.; Larroza, F.; Báez Pressner, J., Cabral, N.; Pereira, M.; Romero, O.; Mallen, G. y Avalos, E., 2019. Caracterización de los Recursos Hídricos para la Gestión de la Protección de la Biósfera del Bosque del Bosque Bosque Mbaracayu (Departamento Canindeyú) y de la Reserva Natural de Tapytá (Departamento de Caazapá) Paraguay. Asunción [En línea]. [s.l.]: CONACYT. [Consulta: 03 de diciembre de 2020]. Disponible en: https://repositorio.conacyt.gov.py/xmlui/bitstream/handle/20.500.14066/2447/14-INV-197.pdf?sequence=1&isAllowed=y
Fernández Rodríguez, E. M., 2020. Métodos analíticos para la determinación de arsénico en arroz. [s.l.]: Universidad Nacional de Educación a Distancia. [Consulta: 29 de julio de 2021] Disponible en: http://e-spacio.uned.es/fez/eserv/bibliuned:master-Ciencias-CyTQ-Emfernandez/Fernandez_Rodriguez_Elena_MariaTFM.pdf
Fretes López, J. C. D. y Díaz Cubilla, F. M. 2014. Estudio de la calidad del agua del Parque Nacional Lago Ypoa y su área de amortiguación. San Lorenzo: Universidad Nacional de Asunción.
Gerdelidani, A. F.; Towfighi, H.; Shahbazi, K.; Lamb, D.T.; Choppala, G.; Abbasi, S.; Fazle Bari, A.S.M.; Naidu, R. y Rahman, M. M. 2021. Arsenic geochemistry and mineralogy as a function of particle-size in naturally arsenic-enriched soils. En: Journal of Hazardous Materials, 403, 123931. DOI: https://doi.org/10.1016/j.jhazmat.2020.123931
El Himri, M.; Errasfa, M.; El Kassimi, A.; Naboulsi, A.; El Himri, A. y El Haddad, M., 2022. Method validation for arsenic speciation in contaminated soil by HPLC-ICP-MS coupling method. En: Journal of the Indian Chemical Society, 99(10), 100684. DOI: https://doi.org/10.1016/j.jics.2022.100684.
Kebonye, N. M.; John, K.; Chakraborty, S.; Agyeman, P. C.; Ahado, S.K.; Eze, P.N.; Němeček, K.; Drábek , O. y Borůvka, L., 2021. Comparison of multivariate methods for arsenic estimation and mapping in floodplain soil via portable X-ray fluorescence spectroscopy. En: Geoderma, 384, 114792. DOI: https://doi.org/10.1016/j.geoderma.2020.114792
Heikens, A., 2006. Arsenic contamination of irrigation water, soil and crops in Bangladesh: risk implications for sustainable agriculture and food safety in Asia [En línea]. Bangkok: FAO. [Consulta: 01 de junio de 2023]. Disponible en: https://www.fao.org/publications/card/es/c/c6936a3e-2998-53d4-830b-f55c91c9887e/
IBM Corp, 2015. IBM SPSS Statistics for Windows. Vers. 2015.23.0. New York: IBM Corp.
International Organization for Standarization, 2017. ISO/IEC 17025: General requirements for the competence of testing and calibration laboratories. Ginebra: ISO.
Ishikawa, K., 2002. Qué es el control total de calidad? La modalidad japonesa. Bogotá: Editorial Norma. ISBN: 958-04-7040-5
Litter, M. I.; Ingallinella, A. M.; Olmos, V.; Savio, M.; Difeo, G.; Botto, L.; Farfán Torres, E. M.; Taylor, S.; Frangie, S.; Herkovits, J.; Schalamuk, I.; González, M. J.; Berardozzi, E.; García Einschlag, F. S.; Bhattacharya, P. y Ahmad, A., 2019. Arsenic in Argentina: occurrence, human health, legislation and determination. En: Science of the Total Environment, 676, pp. 756–766. DOI: https://doi.org/10.1016/j.scitotenv.2019.04.262.
Litter, M. I.; Armienta, M. A. y Farías, S. S., 2009. Metodologías analíticas para la determinación y especiación de arsénico en aguas y suelos [En línea]. Buenos Aires: IBEROARSEN, CYTED. [Consulta: 05 de octubre de 2020]. Disponible en: https://paginas.fe.up.pt/~cigar/html/documents/Monografia2_000.pdf
Martínez, N. D.; Rodríguez, A. M.; Gutiérrez, A. R.; Di Carlo, M. D. y Durán, A. Á., 2018. Determinación de la incertidumbre del método de análisis de aflatoxinas por HPLC en pasa de uva. En: Tecnura, 22(58), pp. 25–36. DOI: https://doi.org/10.14483/22487638.12896.
Mencias Recalde, D. C., 2018. Validación de métodos de ensayo para la determinación de fósforo total, cromo hexavalente y sólidos totales en agua, en el laboratorio ambiental y consultoría ENVIRONOVALAB CÍA. LTDA. Quito: Universidad Central del Ecuador.
Mereles, L., 2017. Validación de un método para la determinación de arsénico inorgánico en muestras de arroz (Oryza sativa) pulido y descascarillado, basada en la detección por espectroscopia de absorción atómica con generador de hidruros, 2017. San Lorenzo: Universidad Nacional de Asunción.
Miller, J. y Miller, J., 2002. Estadística y quimiometría para química analítica. 4 ed. Madrid: Pearson Educación S.A. ISBN:84-205-3514-1.
Rada Mendoza, Maite del Pilar; Alvira, Leydi Fernanda; Hoyos, Olga Lucia y Villada Castillo, Héctor Samuel, 2012. Cuantificación de arsénico por absorción atómica en termoformados y películas flexibles biodegradables. En: Biotecnología en el Sector Agropecuario y Agroindustrial, 10(1), pp. 157–165.
Reid, M. S.; Hoy, K. S.; Schofield, J. R. M.; Uppal, J. S.; Lin, Y.; Lu, X.; Peng, H. y Le, X.C., 2020. Arsenic speciation analysis: A review with an emphasis on chromatographic separations. En: TrAC Trends in Analytical Chemistry, 123, 115770. DOI: https://doi.org/10.1016/j.trac.2019.115770
Senila, M.; Cadar, O. y Miu, I., 2020. Development and validation of a spectrometric method for Cd and Pb determination in zeolites and safety evaluation. En: Molecules, 25(11), 2591. DOI: https://doi.org/10.3390/molecules25112591
Tafur Yépez, C. D., 2014. Validación de un método para análisis de arsénico en agua potable por absorción atómica mediante generación de hidruros. Ambato: Universidad Técnica de Ambato.
Vieira, E. C.; Kamogawa, M. Y.; Guimarães Lemos, S.; Nóbrega, J. y Nogueira R., 2005. Decomposição de amostras de solos assistida por radiação microondas: estratégia para evitar a formação de fluoretos insolúveis. En: Revista Brasileira de Ciência do Solo, 29(4), pp. 547–553. DOI: https://doi.org/10.1590/S0100-06832005000400007
Zagal, E. y Sadzawka, A. R., 2007. Protocolo de métodos de análisis para suelos y lodos [En línea]. Chillán: Universidad de Concepción. [Consulta: 22 de marzo de 2018]. Disponible en: http://www.cofes.org.ar/descargas/relas/4_jornada/Protocolos_suelos y_lodos_Sadzawka.pdf


